Aula nº3 – Quantidade em química
Voltar a: 10ºAno – Química
- Quantidade em química
Mole e massa molar
⇒ Para exprimir o número de partículas existente numa dada porção de matéria (que é extremamente grande) usa-se o número de Avogadro ou constante de Avogadro, NA, em homenagem ao físico italiano Amedeo Avogadro, que, pela primeira vez, o determinou experimentalmente.
Amedeo Avogadro (1776-1856)
- Constante de Avogadro, de símbolo L ou NA:
L (ou NA) = 6,02 x 1023 mol-1
⇒ A mole (mol) é a quantidade de matéria (n) que contém tantas partículas (átomos, moléculas, iões, eletrões, etc.) quantos os átomos que existem em 0,012 kg de carbono-12, ou seja, é a quantidade de matéria que contém a constante de Avogadro (NA= 6,022 x 1023 mol-1).
- 1 mol de átomos de He
⇒ 6,02 x 1023 átomos de He
- 1 mol de moléculas de CO2
⇒ 6,02 x 1023 moléculas de CO2
- 1 mol de iões de Cl–
⇒ 6,02 x 1023 iões de Cl–
fonte:http://web.ccead.puc-rio.br
⇒ A mole é a quantidade de matéria que contém tantas entidades quantos os átomos que existem em 0,012 kg de carbono-12. Este isótopo de carbono foi escolhido como padrão de referência.
⇒ A quantidade de matéria (n) que contém o número de Avogadro de unidades estruturais (nomeadamente átomos, moléculas ou iões) designa-se por mole no Sistema Internacional de Unidades (SI), e representa-se simbolicamente por mol.
- A massa molecular relativa (Mr) é a massa de uma molécula e determina-se a partir da massa atómica relativa dos átomos que a constituem.
- A massa de uma mole de substância designa-se por massa molar. Representa-se pelo símbolo M e exprime-se, usualmente, em g mol-1. Tem o valor numérico da massa molecular relativa que se determina a partir de massas atómicas relativas.
⇒ A massa de uma mole de matéria chama-se massa molar (M) e exprime-se, normalmente. em g mol-1 ou g/mol.
M(H2O) = 2 x Ar(H) + Ar(O) = M(H2O) = 2 x Ar(H) + Ar(O) = 18,02 g mol-1
- A massa molar de 1 mol de moléculas tem uma massa numericamente igual à massa molecular relativa, mas expressa em g mol-1.
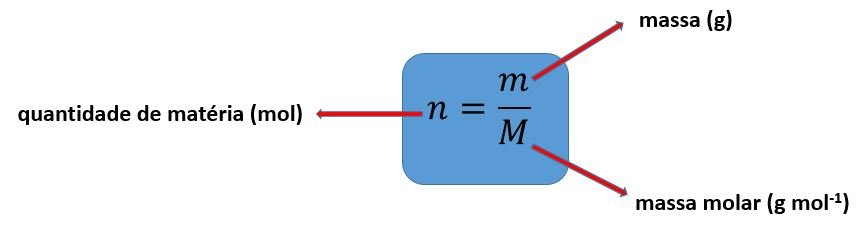
⇒ A quantidade de matéria (n em mol) estabelece a relação entre a massa de uma amostra (m em g) e a sua massa molar (M em g mol-1) :
- A quantidade de matéria (n) que uma dada massa de substância contém é:
- O número de partículas (N) numa amostra obtém-se multiplicando a quantidade de matéria (n) pelo número de Avogadro.
⇒ As partículas existentes em n mol de matéria podem ser átomos, moléculas, iões, eletrões. etc.
- número de partículas (N) de uma substância determina-se por: N = n x NA.
Em resumo: e
→
⇔
Exemplos: (Dados tabelados: Ar(C) = 12,01 e Ar(O) = 16,00)
– A massa molecular relativa do dióxido de carbono, CO2, é:
Mr(CO2) = 1 x Ar(C) + 2 X Ar(O)
Mr(CO2) = 44,01
– A massa molar do dióxido de carbono, CO2, é:
M(CO2) = 44,01 g mol-1
⇒ o que significa que 1 mol de moléculas de dióxido de carbono (ou 6,02 x 1023 moléculas) tem de massa 44,01 g.
Exercícios:
1. Foi medida a massa 3,95 g de permanganato de potássio, KMnO4.
1.1 Que quantidade de matéria de permanganato de potássio foi medida?
1.2 Quantos iões existem nessa amostra?
………………………………………………………………………………………………………………………………………………………………………………………………….
1.1
⇒ M(KMnO4) = 1 x 39,10 + 1 x 54,94 + 4 x 16 = 158,04 g/mol
- n = m/M = 3,95/158,04 = 2,50 x 10-2 mol KMnO4
1.2
⇒ Cálculo do número de moléculas
- n = N/NA ⇔ N = n x NA = 2,50 x 10-2 x 6,02 x 1023 = 1,50 x 1022 moléculas de KMnO4
⇒ Cálculo do número de iões :
- KMnO4 → K+ + MnO4–
⇒ N = 2 x 1,50 x 1022 = 3,01 x 1022 iões
2. O octano, C8H18 (M = 114,26 g mol-1) é um componente da gasolina.
Uma amostra de octano tem 0,30 mol de moléculas.
2.1 Calcula a massa da amostra.
2.2 Calcula o número de moléculas de octano existentes na amostra.
2.1
- n = m/M ⇔ m = n x M = 0,30 x 114,26 = 34 g de C8H18
2.2
⇒ Cálculo do número de moléculas
- n = N/NA ⇔ N = n x NA = 0,30 x 6,02 x 1023 = 1,8 x 1023 moléculas de C8H18
3. Num cristal de enxofre com 5,03 g existem 0,0196 mol de moléculas de enxofre.
3.1. Calcula a massa molar das moléculas de enxofre.
3.2. Determina a fórmula química do enxofre.
3.1 M = 257 g / mol
- n = m/M ⇔ M = m/n = 5,03/0,0196 = 257 g mol-1 de enxofre
3.2
- Ar (S) = 32,07
⇒ 257 = Y x 32,07
- Y = 8
⇒ Assim, a fórmula química do enxofre é S8
4. A fórmula molecular de um ácido orgânico é C2H4O2.
Seleciona a opção correta.
(A) 2,0 mol deste ácido contêm 8,0 mol de átomos.
(B) Em 60,0 g deste ácido existem 1,2 x 1024 átomos de oxigénio.
(C) A massa de 30,0 g deste ácido contém 4,0 mol de átomos de hidrogénio.
(D) Em meia mole de ácido existem 6.0 g de carbono.
- Opção (B)